5 giugno 2024
È il 17 febbraio 2022, data salita agli onori della cronaca contemporanea per essere stata la data di riapertura delle ostilità tra la Russia e l’Ucraina.
A fare le spese di questa guerra insensata e atroce non sono soltanto le popolazioni dei due schieramenti, storicamente sorelle, legate da antichissimi rapporti culturali (ricordo che il Rus' di Kiev fu il nucleo che avrebbe dato alla luce il futuro Impero Russo) e stremate da quasi un anno di guerra; ma anche il patrimonio culturale che soprattutto in Ucraina è stato fortemente danneggiato dai bombardamenti Russi; ne è un esempio il teatro di Mariupol [immagine di copertina], che è stato quasi completamente raso al suolo.
Per dare un'idea della gravità dei danneggiamenti al patrimonio culturale ucraino, stando a dati UNESCO, si tratterebbe di oltre 150 siti danneggiati di cui 45 nella sola regione di Donetsk, 40 nella sola regione di Charkiv e 26 nella regione di Kiev; tra cui edifici storici e religiosi, centri culturali, monumenti, musei e biblioteche. Essi non sono solo piccoli danneggiamenti dovuti a ”necessità militari” ma deliberati attacchi all’identità culturale di un intero popolo

Per comprendere completamente la gravità degli atti commessi in Ucraina, prendiamo in considerazione la sentenza della Corte Penale Internazionale dell'Aja riguardo Ahmed Al Faqi Al Mahdi, in cui è stato evidenziato che:
Dirigere intenzionalmente un attacco contro monumenti storici ed edifici dedicati al culto costituisce un crimine di guerra.
Inoltre la corte ha anche spiegato che:
Ciò che rende questo crimine così grave è il fatto che si tratta di un profondo attacco all’identità, alla memoria e, quindi, al futuro di intere popolazioni. Si tratta di un crimine contro ciò che costituisce la ricchezza di intere comunità, ed è dunque un crimine che ci impoverisce tutti e danneggia i valori universali che siamo tenuti a tutelare.
Detto ciò appare evidente che le innumerevoli devastazioni contro il patrimonio culturale ucraino non faranno altro che aggiungersi alla lunga lista di crimini di cui la Russia si sta macchiando.
L’arte è parte integrante della cultura di un popolo e vedere quest’arte preda di insensate violenze mi rattrista molto e spero che i resposabili paghino per aver privato un popolo di parte del suo passato e, di conseguenza, di un briciolo del suo futuro; fermo restando che la devastazione più grande sarà comunque l'immane perdita di vite umane che questo conflitto ha prodotto.
-Gioele Rosana
2 giugno 2023
Nel mondo dell'arte contemporanea, Bansky è uno dei nomi più noti e ammirati.
Il suo lavoro, caratterizzato da un mix di ironia e critica sociale, ha conquistato il cuore di molti appassionati di street art. Tuttavia, di recente, un evento ha scosso la comunità artistica: alcuni graffiti di Bansky sono stati rovinati.
Ci sono diverse opinioni su questo argomento, ma personalmente credo che sia un vero peccato che queste opere siano state danneggiate. Bansky è un artista che, attraverso la sua arte, è riuscito a portare alla luce problemi sociali e politici che spesso vengono ignorati. I suoi graffiti non sono solo delle belle immagini, ma sono anche messaggi che invitano alla riflessione e alla discussione. Il fatto che qualcuno abbia deciso di rovinare queste opere è un segnale di mancanza di rispetto per l'arte e per il lavoro degli artisti che cercano di comunicare attraverso di essa. Inoltre, questo evento solleva la questione del valore che la società attribuisce all'arte urbana. Spesso gli artisti di strada vengono considerati dei vandalici, quando in realtà il loro lavoro può essere altrettanto significativo e importante di quello degli artisti che espongono in gallerie.È vero che i graffiti di Bansky, come tutte le opere d'arte, non sono eterni. Il tempo e le intemperie possono danneggiarli, ma questo non giustifica il fatto che qualcuno abbia deciso di distruggerli volontariamente. Ci sono modi per preservare l'arte urbana, come ad esempio la creazione di spazi dedicati a questo tipo di arte, dove gli artisti possono esporre le loro opere senza il rischio di essere vandalizzati.In conclusione, i graffiti di Bansky rovinati sono un evento triste e sfortunato.
Tuttavia, questo evento ci invita a riflettere sull'importanza dell'arte urbana e sulla necessità di proteggere e preservare questo tipo di arte. Speriamo che in futuro la società possa apprezzare sempre di più l'arte di strada e che gli artisti possano continuare a comunicare attraverso le loro opere senza il rischio di essere vandalizzati. Un omaggio a Oscar Wilde dipinto sulla prigione di Reading, dove lo scrittore era stato rinchiuso, è stato vandalizzato. Il dipinto rappresentava un uomo vestito da galeotto che si calava con una corda fatta con lenzuola annodate e spinto verso il basso da una macchina da scrivere. L’elemento vandalizzato è stata la macchina da scrivere, cancellata completamente. Sotto il dipinto è stato lasciato un tag a nome “Team Robbo”, riferimento a un celebre sprayer morto nel 2014. Il Ministero di Giustizia britannico, proprietario della prigione, non ha commentato l’episodio. La compagnia teatrale locale Rabble Theatre ha accusato le autorità di non aver fatto nulla per proteggere l’opera d’arte. La comunità di Reading è stata colpita dalla notizia del vandalismo, ma secondo le autorità locali, era “probabilmente destinato ad accadere”. Un esperto di arte urbana ha commentato che l’azione del Team Robbo è stata estemporanea e che un buon restauratore d’arte potrebbe far sembrare il dipinto relativamente simile all’originale, ma ciò costerebbe denaro che esce dal bilancio di Reading.
-Tommaso Giacchi
30 maggio 2023
I vulcani: un mondo in costante cambiamento








27 maggio 2023
Sistematica dei minerali
Le rocce più comuni della crosta terrestre sono costituite da una trentina di minerali, che si classificano in base all'anione che caratterizza il minerale. I minerali sono quindi divisi in: solfuri, alogenuri, ossidi, carbonati, solfati e silicati.
Il gruppo di gran lunga più abbondante sulla Terra è quello dei silicati, caratterizzati dallo ione silicato a geometria tetraedrica. I silicati sono suddivisi in sette gruppi principali:
- nesosilicati a tetraedri isolati;
- sorosilicati a coppie di tetraedri;
- ciclosilicati ad anelli;
- inosilicati a catena singola; -inosilicati a catena doppia; -fillosilicati a piani paralleli; - tettosilicati a struttura tridimensionale.
In base alle loro caratteristiche chimiche e fisiche possiamo suddividere i silicati in due grandi categorie:
- minerali femici, hanno basso rapporto tra gli atomi di Si e O, sono scuri, hanno densità elevata e alta concentrazione di magnesio e ferro;
- minerali sialici, hanno alto rapporto tra gli atomi di Si e O, sono chiari e hanno densità minore.
Infine, l'8% della crosta terrestre è costituito da minerali non silicati, tra cui i più importanti sono: i carbonati, i solfati e alogenuri, gli ossidi e idrossidi, i solfuri, gli elementi nativi.
Introduzione allo studio delle rocce
I minerali sono per la maggior parte aggregati tra loro a formare le rocce. In base al processo di formazione è possibile dividere le rocce in tre grandi gruppi:
- le rocce magmatiche, divise in effusive (che derivano dalla solidificazione della lava) e intrusive (che derivano dalla solidificazione del magma);
- le rocce sedimentarie, derivate dall'accumulo e diagenesi di detriti di varia origine;
- le rocce metamorfiche, derivate dalla trasformazione di rocce preesistenti sottoposte a temperatura e pressione elevate.
Attraverso il processo litogenetico, le rocce possono passare da un gruppo genetico a un altro, passando attraverso differenti processi.
Il riconoscimento di una roccia si basa essenzialmente sul tipo di composizione e di tessitura che essa possiede.
La composizione, che può essere intesa come chimica o mineralogica, si determina riconoscendo i minerali presenti.
La tessitura invece è la disposizione spaziale dei minerali, la loro forma e le loro dimensioni.
-Cinnirella Matteo e Gabriel Basile
Fonti:
https://www.rocks.unipr.it/classificazione/
https://encrypted-tbn0.gstatic.com/images?q=tbn:ANd9GcRmERIaIms0ZiwXjCXA4R75vBs2uNd6R6eqyg&usqp=CAU
https://encrypted-tbn0.gstatic.com/images?q=tbn:ANd9GcSOb3idZ9xwgwz06z8xpDe4soNKfWp7WY85nA&usqp=CAU
https://encrypted-tbn0.gstatic.com/images?q=tbn:ANd9GcSa7g8f18Bq9cdCAjK9ebqS6qJHQSVHBxPs1g&usqp=CAU
https://encrypted-tbn0.gstatic.com/images?q=tbn:ANd9GcSBU3lt8LW_EcPRPmfABSgl1AU9P5uPJ6M-lA&usqp=CAU
25 maggio 2023
INTRODUZIONE SUI MINERALI E LE ROCCE
- COS'È UN MINERALE?
Un minerale è una sostanza solida naturale e avente una composizione chimica ben definita espressa da una formula chimica.
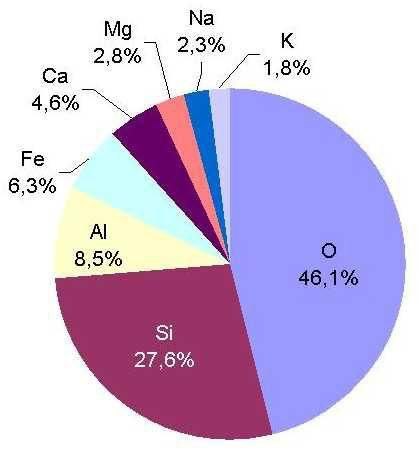
La crosta terrestre è costituita quasi per il 90% da quattro elementi chimici: ossigeno, silicio, alluminio e ferro
I minerali possono formarsi in modi diversi:
• molti si formano per raffreddamento dal magma, una massa di materiali rocciosi allo stato fuso che contiene in soluzione anche sostanze gassose
• altri si depositano per precipitazione da acque ricche di sali, talvolta per azione di organismi viventi
• alcuni possono derivare dalla trasformazione di altri minerali sottoposti ad alte temperature o pressioni (metamorfismo).
- LA STRUTTURA CRISTALLINA DEI MINERALI
Ogni minerale si presenta come un solido dotato di una particolare forma geometrica definita abito cristallino
L'abito cristallino di un minerale è la forma in cui si accrescono i singoli cristalli o gli aggregati dei cristalli, rappresenta il modo in cui sono disposte nel reticolo cristallino e le condizioni in cui si è originato un minerale determinando la forma con cui si accrescono i suoi cristalli
Ogni minerale può presentare uno o più abiti cristallini caratteristici.
Alla forma esterna corrisponde, all'interno, una ben definita disposizione spaziale delle specie atomiche e molecolari costituenti. Questa disposizione spaziale può variare da minerale a minerale.
Le posizioni di atomi, ioni, molecole in un cristallo invece si rappresentano con una serie di punti che definiscono una figura geometrica tridimensionale detta reticolo cristallino.
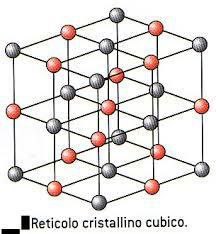
I minerali, pur avendo una struttura interna cristallina, non hanno sempre la stessa forma esterna né questa è sempre la forma di un solido geometrico regolare. La forma esterna dipende in larga parte dalle condizioni in cui i minerali si formano e dalla possibilità di svilupparsi liberamente nello spazio circostante.

Le posizioni degli ioni nella struttura cristallina sono definite e non sono intercambiabili. Uno qualsiasi dei tanti cubetti uguali che costituiscono un cristallo di salgemma è la cella elementare del cristallo di salgemma.
La cella elementare è la più piccola unità tridimensionale che conserva sia la composizione chimica sia la struttura cristallina di quel particolare minerale. I vertici delle celle elementari sono detti nodi del reticolo cristallino. In base al tipo di particelle che occupano i nodi del reticolo cristallino e all'intensità delle forze di attrazione esistenti fra queste, i cristalli si possono classificare in ionici, covalenti, metallici e molecolari.
I cristalli ionici, sono costituiti da cationi e anioni, che si alternano nel reticolo, come nel salgemma
I cristalli covalenti sono costituiti da atomi legati covalentemente fra loro a formare una rete che si estende in tutte le direzioni del cristallo.
I cristalli metallici sono costituti da cationi circondati da elettroni di valenza in movimento e diffusi in tutto il solido. Possiamo trovarli nei metalli nativi come l'oro (Au) e il rame (Cu).
I cristalli molecolari sono costituiti da atomi e da molecole neutre tenute insieme da forze deboli.
- COSA INFLUENZA LA STRUTTURA DEI MINERALI
L'effettiva possibilità che un minerale ha di formarsi in natura è determinata da parametri fisici e chimici:
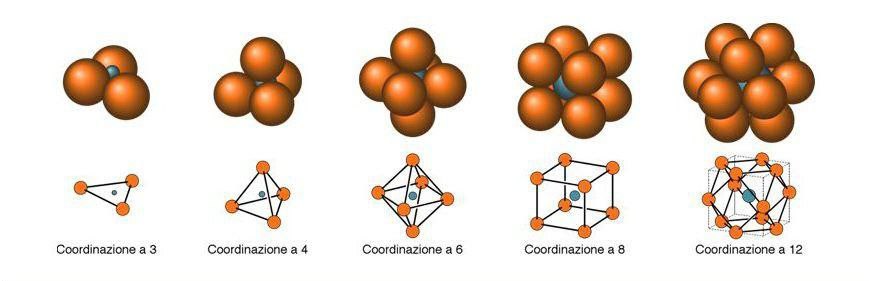
- Parametri fisici: le dimensioni delle specie chimiche che si combinano devono essere tali da poter costituire una struttura cristallina stabile. Le dimensioni relative degli ioni determinano la loro posizione nel reticolo cristallino; gli ioni tendono a disporsi in modo che la loro distanza sia minima a causa della reciproca attrazione. Se ioni positivi e negative hanno dimensioni diverse, intorno a quello piccolo (+) possono posizionarsi solo tre ioni (-) di dimensione maggiore; questa disposizione è detta coordinazione a tre.Se mano a mano la differenza di dimensione degli ioni positivi e negativi diminuisce, la coordinazione diventa a quattro, a sei, a otto e infine a dodici (dimensioni ioni quasi uguali).
- Parametri chimici: le cariche positive e negative devono bilanciarsi perfettamente, affinché la cella elementare sia elettricamente neutra. Se gli ioni di segno opposto non hanno lo stesso numero di cariche, gli altri ioni, con numero di cariche minore, sono presenti in quantità maggiore così da bilanciare esattamente le cariche di segno opposto.
- COME SI FORMA UN MINERALE
Quasi tutti i minerali (a eccezione di quelli amorfi) si formano attraverso un processo di cristallizzazione, cioè il passaggio da un insieme disordinato di atomi a quello ordinato tipico del reticolo cristallino, che determina poi la struttura caratteristica di ciascun minerale.
- Cristallizzazione per raffreddamento di un materiale fuso (per esempio la lava eruttata da un vulcano). Gli atomi o i gruppi di atomi si aggregano per formare i reticoli cristallini tipici dei composti chimici che possono formarsi a seconda della natura del fuso.
- Precipitazione da soluzioni acquose calde in via di raffreddamento. Al diminuire della temperatura, si formano via via cristalli di specie mineralogiche diverse, a seconda della composizione chimica della soluzione.
- Sublimazione di vapori caldi. Le esalazioni vulcaniche, per esempio, possono determinare la formazione di cristalli su superfici relativamente fredde vicine alla zona di fuoriuscita dei vapori.
- Evaporazione di soluzioni acquose, soprattutto acque marine.
- Attività biologica, che porta alla costruzione di gusci o apparati scheletrici.
- PROPRIETÀ FISICHE DEI MINERALI
I minerali hanno delle proprietà fisiche che aiutano al loro riconoscimento. Queste proprietà sono:
- Colore;
- Colore della polvere;
- Densità;
- Sfaldatura;
- Durezza;
- Lucentezza;
- Temperatura di fusione.
Il colore
Il colore è la prima proprietà di un minerale che viene presa in considerazione, perché in risalto.
Il colore di un minerale è funzione della sua composizione chimica. Il colore dei minerali è dato fondamentalmente da ferro, cromo, manganese, cobalto, nichel, rame.
Inoltre in alcuni minerali della stessa specie il colore può cambiare in base alle impurezze presenti, anche se presenti in piccolissime quantità. Un esempio classico è il quarzo che può essere bianco, rosa, azzurro, violetto e addirittura fumeè.
Il colore della polvere
Se lo stesso minerale può essere di vari colori, la sua polvere ha sempre lo stesso colore. Un esempio è l'apatite, che può essere verde o marrone, che ha sempre la polvere di colore bianco.
Una tecnica molto utile per vedere il colore della polvere di un minerale è il metodo dello striscio.
Se strofiniamo un minerale su una superficie abrasiva otteniamo una striscia di polvere fine, della quale se osserviamo il colore otteniamo un utile strumento nel riconoscimento del minerale.

Densità
Ogni minerale ha una densità diversa. Infatti se prendi in mano due campioni, delle stesse dimensioni, di due minerali diversi noterai che hanno un peso diverso.
Sfaldatura
La sfaldatura è la proprietà che hanno alcuni minerali di rompersi preferibilmente lungo certe direzioni.
All'interno di una struttura cristallina, la sfaldatura si verificherà secondo le direzioni lungo le quali i legami chimici interatomici sono più deboli. Minerali con sfaldatura particolarmente facile sono ad esempio le miche, gli anfiboli e i pirosseni, la fluorite e la calcite.
Un minerale può mostrare una o più direzioni di sfaldatura, per le quali si usano gli aggettivi che descrivono la maggiore o minore facilità di ottenerle. Si parlerà di sfaldatura perfetta, buona, imperfetta, difficile o assente. Se tale direzione preferenziale di rottura non è evidente, quindi il minerale si rompe secondo superfici irregolari, si parla allora di frattura.

Durezza
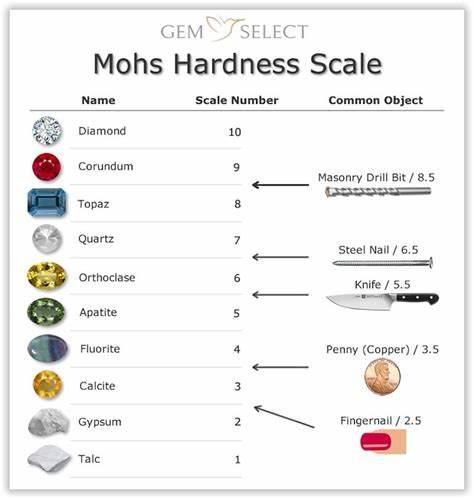
La durezza di un minerale è una misura della sua resistenza a essere scalfito e abraso. La durezza dei minerali è determinata mediante comparazione con la scala di Mohs. Questa scala è costituita da 10 minerali disposti in ordine crescente di durezza.
La durezza viene determinata con strumenti di laboratorio, come ad esempio lo sclerometro, che misurano la resistenza dei minerali e che fanno riferimento a scale di valori assolute derivate dalla scala di Mohs.
Lucentezza
La lucentezza di un minerale dipende dal modo con cui la luce è riflessa o rifratta, così come dalla qualità della superficie di un cristallo.
Si distinguono i minerale con lucentezza metallica e lucentezza non metallica.
I minerali metallici opachi (pirite, galena etc) hanno un forte potere riflettente perciò hanno una lucentezza metallica. Invece minerali come la blenda e il rutilo hanno una lucentezza difficile da definire.
Temperatura di fusione
È il valore di temperatura in cui il minerale passa dalla fase cristallina alla fase liquida e assume un valore specifico in ogni minerale.
6.POLIMORFISMO E ISOMORFISMO
- Polimorfismo:è un fenomeno dei materiali cristallini e descrive la capacità di una sostanza di esistere come due o più fasi cristalline diverse. È stato trovato che una medesima sostanza semplice o composta, può cristallizzare in due o più diverse forme cristalline classificate in sistemi cristallografici diversi, ciascuna delle quali è stabile entro determinati limiti di pressione e di temperatura.
- Isomorfismo: è il fenomeno per il quale due o più sostanze diverse cristallizzano separatamente per dare cristalli con caratteri geometrici molto simili, è detto isomorfismo. Due o più sostanze isomorfe possono cristallizzare insieme formando soluzioni solide, ovvero se un sistema di dette sostanze è portato allo stato fuso o in soluzione e poi o si raffredda il fuso o si fa evaporare il solvente, si ottengono dei cristalli che sono detti cristalli misti.
- SOLIDI AMORFI
La quasi totalità dei minerali è allo stato cristallino. Esistono però dei casi in cui i minerali hanno una struttura disordinata, in questo caso, i minerali vengono detti amorfi o vetrosi.
In un solido amorfo, gli atomi o le molecole non sono disposti in modo regolare, ma sono distribuiti casualmente in tutto il materiale, rendendo difficile identificare un pattern o una struttura ben definita. Questo fa sì che i solidi amorfi siano spesso descritti come "vetroso", perché il loro aspetto ricorda quello del vetro.
I passaggi di stato solido-liquido consentono di distinguere una sostanza amorfa da una cristallina: la fase cristallizzata ha un punto di fusione netto, mentre la fase amorfa non ha un punto di fusione ben definito, per cui all'aumentare della temperatura diventa prima pastosa e molle, poi più fluida e infine liquida. Se la fase liquida di certe sostanze non è raffreddata con molta lentezza, il movimento delle particelle diminuisce bruscamente e queste rimangono «imprigionate» in uno stato solido disordinato.
Esempi di solidi amorfi includono il vetro, la gomma, alcuni tipi di plastica, la cera e molti materiali biologici come il collagene e la cheratina. La loro mancanza di struttura cristallina conferisce loro proprietà fisiche e chimiche uniche, che li rendono utili in diverse applicazioni industriali e tecnologiche.

-Carola Barbato, Laura Platania
25 maggio 2023
Rocce ignee
Le rocce ignee possono essere suddivise in intrusive ed effusive. L'attribuzione di una roccia ad una delle sue categorie è basata sulla tessitura.

La tessitura è l'espressione del grado di cristallinità e della dimensione dei cristalli presenti in una roccia .
Quando il raffreddamento si protrae per lungo tempo e sotto forte pressione litostatica, il magma riesce a conservare i suoi componenti volatili, come ad esempio gas vari che favoriscono la cristallizzazione.
Le rocce intrusive sono completamente cristalline, hanno una grana più grossolana, potendo vedere anche i diversi cristalli ad occhio nudo.
Quando invece il magma fuoriesce in superficie data la rapidità del raffreddamento, si formano invece cristalli molto piccoli o addirittura rocce vetrose cioè prive di cristalli.
Nelle rocce effusive vi possono essere anche cristalli isolati di maggiore dimensione, distinguibili ad occhio nudo, i fenocristalli. Questa tessitura è detta tessitura porfirica.
Le rocce ignee inoltre si suddividono in chiare o scure :
- le rocce chiare sono dette sialiche e sono ricche di quarzo e feldspato.

- le rocce scure invece sono dette femiche e sono ricche di anfiboli, pirosseni e olivina. Tutti minerali a base di magnesio e ferro.

Si dicono invece ultrafemiche le rocce costituite solamente da pirosseni e olivina

Le rocce ignee nel sottosuolo
I corpi magmatici che si sono consolidati nel sottosuolo sono detti plutoni.

I plutoni hanno forma e dimensioni variabili e possono inserirsi in vario modo tra le rocce preesistenti.
I batoliti invece sono i plutoni maggiori e si estendono per centinaia o migliaia di kilometri quadrati, nel caso di dimensioni minori si parla di ammassi o masse satelliti.

I batoliti costituiti da graniti e granodioriti formano l'ossatura dei continenti e si trovano al centro delle grandi catene montuose. Le rocce che derivano dal processo di anatessi sono chiamate graniti anatettici.
L'anatessi è un fenomeno molto importante e riguarda la spiegazione della grande abbondanza di rocce granitiche.
Alcuni corpi plutonici di dimensioni medio-piccole possono solidificare a bassa profondità quando il magma riesce ad aprirsi fino alla superficie. Questi corpi plutonici iniettati possono infilarsi nelle rocce incassanti in modo concordante ovvero parallelo con gli strati delle rocce sedimentarie oppure in modo discordante.
L'intrusione dei corpi concordanti può avvenire in due modi:
I filoni-strato sono corpi concordanti di forma tabulare.

Essi si distinguono da una normale colata lavica per due caratteristiche:
Anche i laccoliti si formano come i filoni-strato, ma invece di essere tabulari sono convessi verso l'alto.

I tipici laccoliti italiani sono quelli dei Colli Euganei.

I corpi discordanti, detti dicchi o filoni , sono di forma tabulare e tagliano secondo vari angoli la stratificazione delle rocce incassanti. Si inseriscono lungo fessure aperte dell'iniezione magmatica o nelle fratture già esistenti. Lo spessore dei dicchi varia da pochi centimetri a parecchie decine di metri

Link foto:
https://images.app.goo.gl/98P6N59k2tZbXhSE6
https://images.app.goo.gl/Qo2SEEAcNVhFswKt9
https://images.app.goo.gl/NQ8F7p1CDCH48XSCA
https://images.app.goo.gl/Q4hgsbuLucJiVCoe9
https://images.app.goo.gl/zWhSK191NfbndcRNA
https://images.app.goo.gl/UaAf1fKDxWH633Xs5
https://images.app.goo.gl/xiotR7z1xm7LuZj49
https://images.app.goo.gl/53r5tJCuB8wv8Gyh7
https://images.app.goo.gl/tuBvm1guSfPse6FZ7
https://images.app.goo.gl/nyjJctvnFYwmj1Bs9
24 maggio 2023
Dal magma alla roccia
4,5 miliardi di anni fa: la terra è nelle fasi iniziali della propria storia. Grazie alla forza di gravità, un’ammasso di materiale allo stato fuso , piano piano diventa il nostro mondo. I materiali si disposero in base alla loro densità : i più leggeri in superficie. Questi furono i primi a raffreddarsi e dal quel momento inizió il processo di solidificazione , che determinò l’associazione di materiali simili tra loro. Così si crearono le rocce più antiche della terra. Queste rocce sono chiamate ignee (dal latino ignis = fuoco) o magmatiche o eruttive , formati dal raffreddamento di magma incandescente, caratterizzato da una temperatura tra i 650° e 1300°.
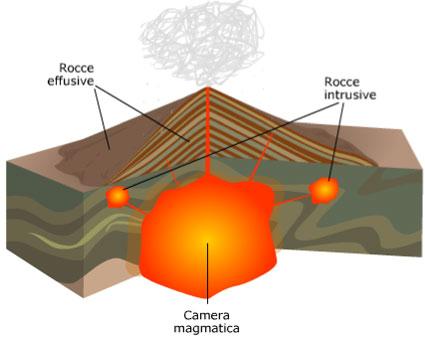
Le rocce ignee costituiscono circa l’80% della crosta terrestre e possono essere distinte in due grandi categorie:
- Le rocce effusive, o vulcaniche, sono originate dalla solidificazione di un magma che fuoriesce sulla superficie terrestre. Per le rocce effusive esiste una classificazione che vede da una parte le rocce effusive sialiche ossia ricche di SiO2 (silice), in una percentuale intorno al 65% e dall'altra le rocce effusive femiche con un contenuto più basso di SiO2 (tra il 42% e il 55%).

- Le rocce intrusive, o plutoniche, sono originate dalla solidificazione per lento raffreddamento di un magma che ristagna all’interno della crosta. Le intrusive si dividono in:
- Rocce soprassature o granitoidi: In questo campo le rocce contengono una percentuale minima di quarzo del 20%, come : alicaligranito, granito, granodiorite, tonalite
- Rocce sature: percentuale di quarzo compresa tra lo 0 e il 5%. Come: alcalisienite, sienite, monzonite, monzodiorite e monzogabbro, diorite e gabbro
- Rocce sottosature: contengono feldspatoidi ( I feldspatoidi sono una famiglia di silicati comuni specialmente nelle rocce effusive). Non contengono invece quarzo. Queste sono: nefelinsienite,plagiosenite,theralite.

- Le rocce filoniane o ipoabissali o subvulcaniche sono un tipo di rocce magmatiche che cristallizzano interamente o in gran parte a modesta profondità, in corpi di varia forma ma quasi sempre di ridotte dimensioni


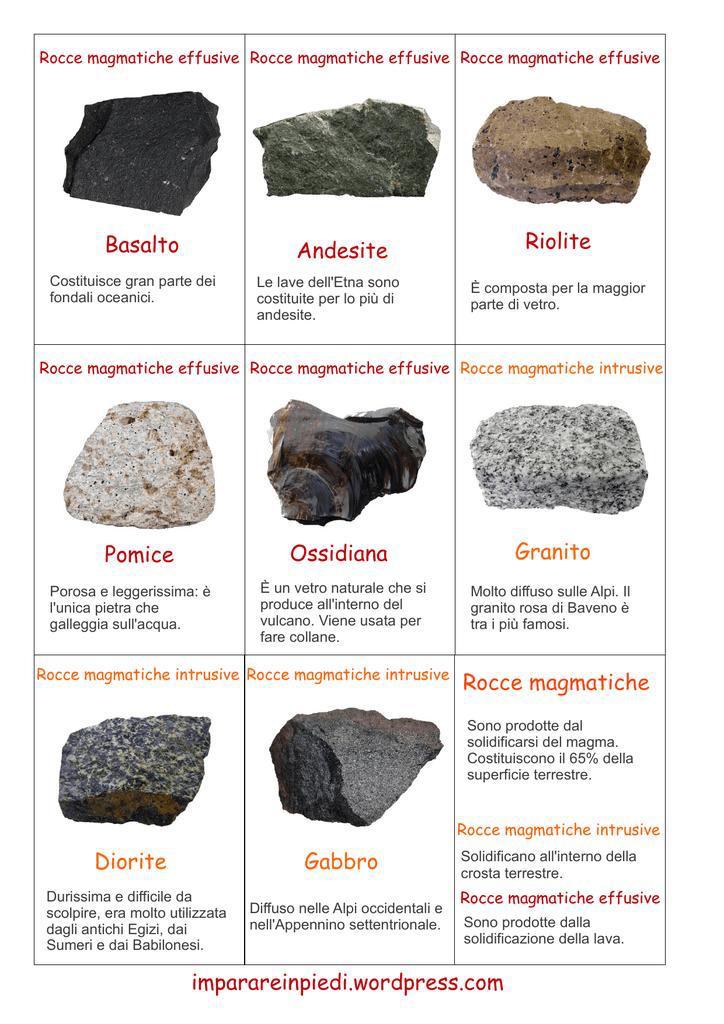
Info point : definizione di magma : una massa di materiali rocciosi allo stato fuso, contenente in soluzione anche sostanze allo stato gassoso.
Magma
La temperatura è variabile tra 650 e 1300 °C. I valori più bassi delle temperature si registrano solitamente nei magmi ricchi in silice SiO2 , quelli più elevati nei magmi poveri si SiO2 ( lava dei vulcani). Quando il magma arriva in superficie , questo perde i gas e diventa lava.
Quindi in magma presenta caratteristiche diverse quando fuoriesce dalla crosta terrestre , ma anche durante la risalita subisce vari cambiamenti chimici e fisici. Infatti oltre alla diminuzione della pressione litostatica , si ha anche un raffreddamento che porta alla separazione e alla cristallizzazione di alcuni elementi chimici mentre altri elementi possono essere prelevati dalle rocce della crosta terrestre.
I principali fattori fisici che portano alla formazione delle rocce sono:
- aumento di temperatura
- riduzione della pressione
- aumento del contenuto di acqua
Info point: ancora oggi sotto lo strato roccioso in cui noi poggiamo i nostri piedi si estende materiale allo stato solido per circa 3000 km. Man mano che si procede al di sotto della superficie terrestre, la temperatura aumenta. Ma oltre alla temperatura aumenta anche la pressione dovuta al peso esercitato dagli strati rocciosi sovrastanti.
La pressione esercitata dalle rocce in tutte le direzioni dello spazio è detta pressione litostatica.
Nella astenosfera, (sottile strato fluido-viscoso, situato al disotto della crosta terrestre, ad una profondità compresa tra 100 e 300 km. )le temperature sono comprese fra 1000o e i 1500° ma ogni minerale ha un suo punto di fusione influenzato da molti fattori ad esempio l’olivina fonde 1600o e 1800° ma per effetto delle rocce sovrastanti la temperatura di fusione aumenta : quindi se la pressione aumenta si alza di conseguenza il punto di fusione. Al contrario una piccola quantità d’acqua nel magma può far abbassare la temperatura alla quale silicati rimangono allo stato fuso. questo vuol dire che i magmi contenenti acqua possono avvicinarsi di più alla superficie terrestre sotto forma di lava. Quindi i volatili del magma sono l’acqua e gli altri gas presenti come il diossido di carbonio, lo zolfo ,l’azoto, l’idrogeno, il cloro, il fluoro.
Inoltre sono elementi che rimangono allo stato liquido e gassoso a temperature inferiori di quelle di silicati perciò a temperature inferiori questi si separano, mentre i silicati si cristallizzano.
Importanti caratteristiche fisiche del magma sono:
⁃ viscosità : è la proprietà più importante di un magma. Esprime la resistenza che ogni corpo oppone alle forze che ne vogliono modificare la forma Quindi in parole povere, la viscosità non altro “la resistenza che ha un determinato flusso allo scorrimento”. La viscosità, come le altre proprietà fisiche dei magmi, dipende dalla composizione chimica del magma. Infatti aumenta all’aumentare del contenuto in silice (perché all’interno di un fluido magmatico si vanno a formano legami forti tra il silicio e l’ossigeno), e diminuisce all’aumentare del contenuto di elementi o sostante che vanno ad interrompere tali legami, come ad esempio i volatili disciolti (l’acqua), gli elementi alcalini, il Fe ed il Mg. La viscosità inoltre è inversamente proporzionale alla temperatura, ciò vuol dire che cresce al diminuire della stessa e all’aumentare del contenuto dei cristalli presenti nel fuso magmatico. La presenza di acqua e/ o di fluoro nei liquidi magmatici ne riduce la viscosità.


-Densità: La densità di un corpo, è il rapporto tra la massa ed il volume.La densità di un magma controlla i meccanismi di risalita di un fuso tra le rocce incassanti, nonché i fenomeni di differenziazione e frazionamento che possono verificarsi nella camera magmatica. Questa è in funzione della temperatura, della composizione chimica, della pressione e dal contenuto di gas presenti in un magma. varia da circa
2,2 g/cm3 per i magmi acidi (ricchi di silicio) a circa 2,9 g/cm3 per i magmi basaltici ( poveri di silicio) ;
L’EVOLUZIONE DEI MAGMI
La genesi dei magmi
Il processo fondamentale che porta alla genesi dei magmi, e quindi alle rocce magmatiche, è la fusione parziale di rocce preesistenti.
Per ottenere la fusione della crosta o del mantello è necessario:
•diminuire la pressione; questa condizione avviene in prossimità delle dorsali medio-oceaniche, dove la litosfera e la sottostante astenosfera sono sottoposte a forze di distensione che causano una diminuzione locale di pressione. Essa induce il passaggio allo stato liquido della parte più superficiale dell'astenosfera e quindi la formazione di lave basaltiche. Poiché il punto di fusione del magma basico diminuisce con il diminuire della pressione, quando si avvicina alla superficie, avendo una temperatura di formazione abbastanza elevata, incontra condizioni che ne facilitano il mantenimento allo stato liquido. Sui magmi acidi la pressione ha un effetto opposto, giacché, per mantenere lo stato fuso la temperatura deve aumentare anziché diminuire, per questo solidifica prima di giungere in superficie;
• presenza di acqua, la cui concentrazione influisce abbassando il punto di fusione della roccia( dunque l’abbassamento dei limiti critici di pressione P e temperatura T) .Sotto le dorsali parte dell'acqua può derivare direttamente dal magma, ma la maggior parte proviene dalle acque profonde circolanti;
• aumento di temperatura, che può avvenire in due condizioni. Può verificarsi quando masse rocciose sono trasportate in profondità lungo le zone di subduzione dove le temperature progressivamente più elevate, non controbilanciate dalla pressione, provocano la fusione. Una seconda condizione che dà origine ad un aumento della temperatura è dovuta al calore trasportato verso l'alto in prossimità di correnti convettive presenti nel mantello.
Se la fusione avviene nel mantello (ultrabasico) si forma un magma primario di composizione prossima a quella del basalto, a elevate profondità e ad alta temperatura (1200-1400°C) e molto fluido, tanto da poter risalire in superficie prima di cristallizzarsi. Esso dà origine a gran parte delle rocce effusive ed ipoabissali. I magmi primari derivano da processi di fusione parziale (non oltre il 30%) di rocce del mantello superiore , le cosiddette peridotiti, costituire essenzialmente di olivina e pirosseni, con l'aggiunta di minerali accessori quali spinello, granato, anfibiolo e mica flogopipe.
Se avviene all'interno della crosta continentale, dove, già a qualche decina di km di profondità, la temperatura è elevata abbastanza (600-700°C) da provocare, almeno in certe condizioni, la fusione dei minerali sialici, si formano fusi acidi, detti magmi anatettici attraverso un processo chiamato anatessi ( dal greco anatexis= fusione) con il quale si designa il processo di fusione parziale delle rocce ignee, sedimentarie e metamorfiche. Questi magmi sono molto viscosi poiché sono costituiti da una porzione fusa che contiene molti residui ancora solidi che hanno un punto di fusione più alto. Essi si muovono perciò con notevole difficoltà e non risalgono molto entro la crosta, e tendono a cristallizzarsi in profondità formando i batoliti granitici.
Se si esaminano le rocce magmatiche che costituiscono la crosta terrestre , è evidente la larghissima prevalenza di due tipi di rocce: i graniti (rocce intrusive) e i basalti ( rocce effusive).
Non si tratta di una semplice coincidenza che tra le rocce intrusive siano dominanti quelle sialiche ,cioè quelle in cui il silicio è abbondante, e che tra quelle effusive prevalgano quelle con un elevato contenuto di ferro e magnesio .
Magma granitico : Dati sperimentali hanno dimostrato che i minerali più ricchi di silice fondano a circa 700 °C: dunque quando la crosta raggiunge queste temperature (tra i 30 e i 40 Kmdi profondità) si verifica il processo di anatessi , le rocce fondono parzialmente e danno origine al magma granitico.
Magma basaltico: Invece per ottenere magma basaltico occorre fondere rocce ricche di olivina e pirosseni che si trovano nel mantello o nelle parti più profonde della crosta , fondono tra i 1200 e i 1400 °C , a circa 100 km di profondità
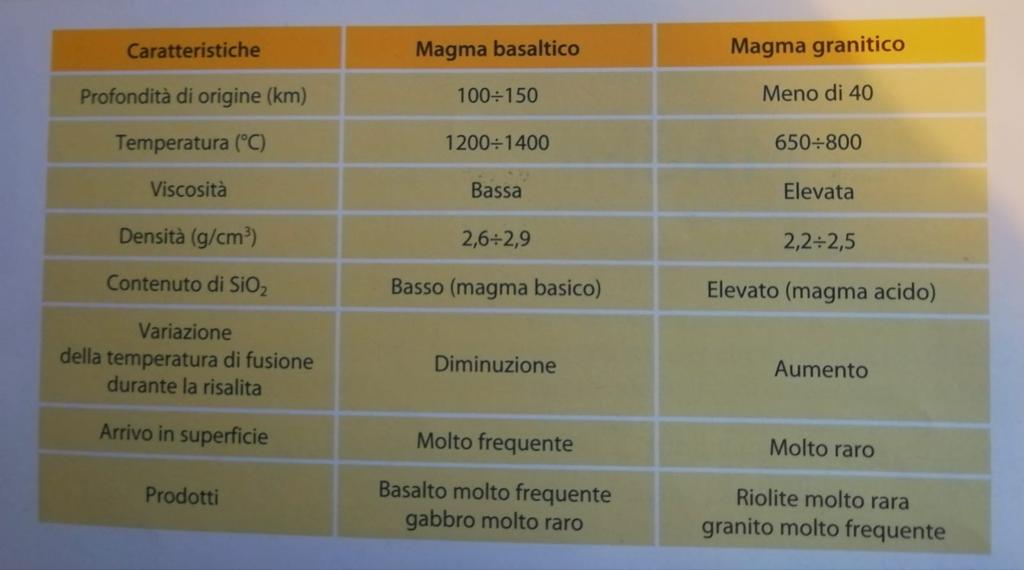
figura: le diverse provenienze dei 2 magmi; quello granitico nasce da una parziale fusione in situ di rocce esistenti, quello basaltico è composto da materiali del mantello o della crosta profonda che salgono per la prima volta in superficie.
Il diverso comportamento dei magmi basaltici e granitici deriva anche dalla diversa influenza che la pressione ha sulla temperatura di fusione:
- la temperatura di fusione del magma granitico aumenta quando diminuisce la pressione
- al contrario, la temperatura di fusione del magma basaltico diminuisce con la diminuzione della pressione .
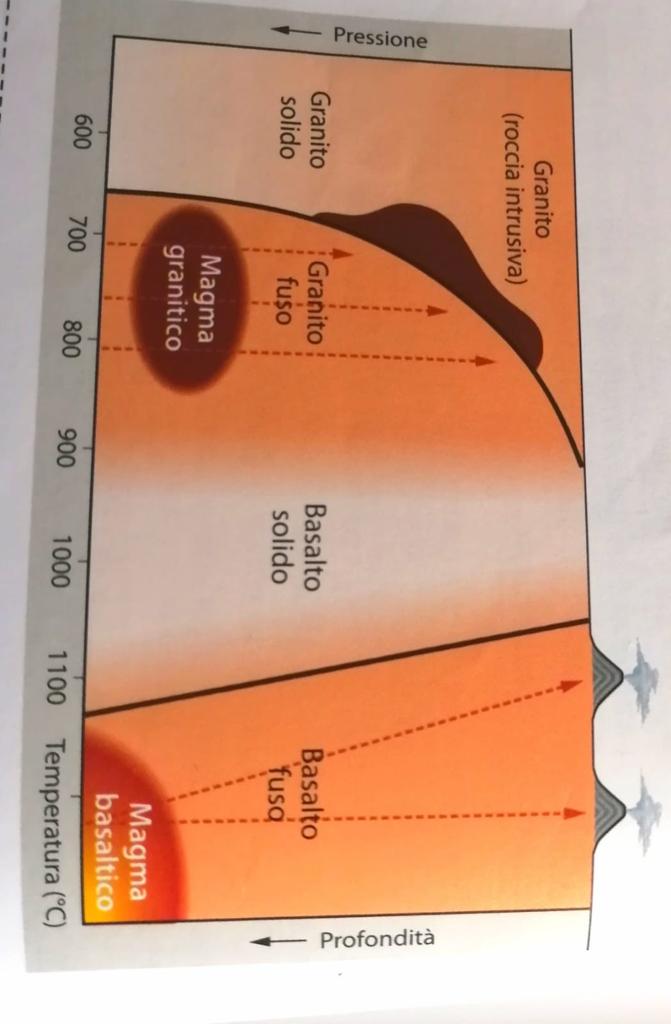
La diminuzione di pressione produce effetti opposti sui magmi granitici e su quelli basaltici: per i primi la temperatura necessaria per mantenere lo stato fluido aumenta, per i secondi diminuisce. La maggior parte dei magmi granitici non giunge in superficie perché solidifica prima, i magmi basaltici giungono allo stato fluido fino alla superficie .
Cristallizzazione magmatica e differenziazione
Un magma basaltico dopo la sua formazione per la fusione della parte superiore del mantello, può risalire direttamente attraverso fessure profonde ed estese, fino ad espandersi come lava sul fondo degli oceani o nel cuore di un continente, dando origine a rocce che rispecchiano la composizione originaria del magma; ma può anche risalire lentamente o per tappe successive, e allora il fuso comincia a frazionarsi, cioè cambia composizione nel tempo dando origine a magmi diversi. Il fenomeno è la cristallizzazione frazionata.
Durante il raffreddamento, infatti, i minerali che si formano non si separano tutti insieme, ma secondo un ordine che dipende dalla temperatura di fusione di ognuno. Se il raffreddamento avviene regolarmente, al diminuire della temperatura si susseguono di volta in volta varie reazioni chimiche, in cui i cristalli del minerale formatosi a temperatura più alta, diventando instabili al diminuire della temperatura, perciò reagiscono con la porzione di magma rimasta ancora fusa entro cui essi galleggiano; il minerale è dunque totalmente riassorbito, mentre si cristallizza un nuovo minerale in equilibrio con la temperatura più bassa; a una temperatura ancora inferiore, anche il nuovo minerale reagisce con il fuso e così via.
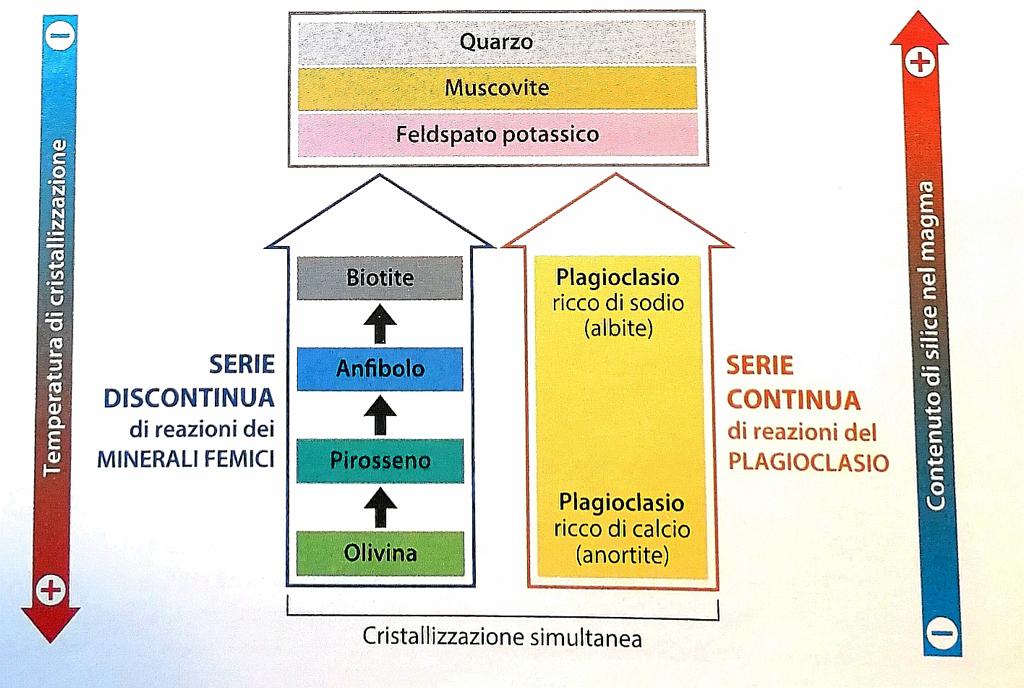
Bowen ha identificato due diverse sequenze, dette serie di Bowen, secondo le quali, per diminuzione della temperatura, si formano i minerali fondamentali delle rocce magmatiche.
• La serie continua, così detta perché si ha un passaggio graduale da un minerale ad un altro, porta alla separazione dal fuso dei plagioclasi. Si tratta di un gruppo di minerali costituiti da miscele solide, in tutte le proporzioni, di due termini “puri”: l'albite (silicato ricco di sodio) e l'anortite (silicato ricco di calcio).Quando inizia la cristallizzazione, cominciano a formarsi cristalli a composizione ricca di anortite ma, col progredire del raffreddamento, i cristalli già formati cominciano a reagire col fuso, trasformandosi in altri cristalli via via più ricchi di albite. La composizione della miscela finale dipende dalla composizione del fuso iniziale: più questo è acido, più il plagioclasio che alla fine si forma è ricco in albite.
• Contemporaneamente alle reazioni della serie continua si svolgono, in modo del tutto indipendente, le reazioni della serie discontinua, con passaggio repentino da un minerale ad un altro, che portano alla separazione del fuso dei minerali femici. In un basalto, per esempio, il minerale che si forma per primo è l'olivina, silicato ricco di ferro e magnesio. Cristalli di olivina rimangono sparsi nel fuso per un certo intervallo di temperatura, al termine del quale reagiscono tutti con una parte del liquido per formare i pirosseni, silicati più ricchi di silicio e contenenti calcio, potassio e magnesio; anche questi ultimi, a temperatura inferiore, reagiscono con il liquido residuale per formare gli anfiboli, silicati contenenti acqua. E così via. Anche per la serie discontinua quanto più il fuso iniziale è acido, tanto più avanti si spinge la serie di reazioni, fino alla biotite, che è l'ultimo minerale che si può formare in tale serie.
Al termine delle due serie, un'ulteriore diminuzione della temperatura porta la formazione di feldspato potassico, muscovite e quarzo.
Solo a solidificazione completa la roccia mostrerà una composizione corrispondente a quella del magma iniziale; se il magma è acido ne risulterà una roccia a composizione granitica, mentre se è basaltico le reazioni si arrestano prima, formando rocce femiche. Tutto questo si verifica se la cristallizzazione avviene in modo continuo; tuttavia, se qualche fenomeno interrompe la regolarità della cristallizzazione, come per esempio se ad un certo punto movimenti nella crosta fanno allontanare il fuso residuale, molto fluido, dalla massa già cristallizzata, quando il fuso migrato riprenderà a cristallizzare, non potendo più reagire con i minerali già formati, darà origine a minerali più sialici. Poiché i minerali che si separano per primi (a più alte temperature) sono quelli più femici, il fuso residuale risulterà indirettamente sempre più arricchito in silice e alcali, cioè sempre più differenziato in senso acido. Tutto questo si verifica se la cristallizzazione avviene in modo continuo; tuttavia, se qualche fenomeno interrompe la regolarità della cristallizzazione, come per esempio se ad un certo punto movimenti nella crosta fanno allontanare il fuso residuale, molto fluido, dalla massa già cristallizzata, quando il fuso migrato riprenderà a cristallizzare, non potendo più reagire con i minerali già formati, darà origine a minerali più sialici. Poiché i minerali che si separano per primi (a più alte temperature) sono quelli più femici, il fuso residuale risulterà indirettamente sempre più arricchito in silice e alcali, cioè sempre più differenziato in senso acido.
sitografia:
https://it.wikipedia.org/wiki/Roccia_magmatica
https://manualedelgeologo.it/sienite/
https://it.m.wikipedia.org/wiki/Roccia_effusiva
https://it.m.wikipedia.org/wiki/Roccia_filoniana
https://it.m.wikipedia.org/wiki/Roccia_intrusiva
https://it.m.wikipedia.org/wiki/Feldspatoide
https://tinyurl.com/539m8rt2
https://www.intrageo.it/geologia/vulcanologia/le-proprieta-fisiche-dei-magmi/
Elaborato di Fontana Giulia, Fazzino Giorgia 4D 2022/2023.
23 maggio 2023
L'attività vulcanica comprende eruzioni esplosive ed effusive. Durante le eruzioni esplosive, il magma, contenente gas dissolti, viene espulso ad alta velocità, generando la caduta gravitativa di frammenti di roccia e cenere verso il suolo. Le colate piroclastiche, flussi incandescenti di gas, cenere e frammenti di roccia, si spostano rapidamente lungo i fianchi del vulcano, rappresentando una minaccia mortale. L'onda basale è un'onda d'urto generata dall'espansione dell'aria e compressione causata dalla rapida espulsione di gas e frammenti di roccia. Durante l'attività vulcanica effusiva, il magma fuoriesce in modo relativamente tranquillo attraverso fessure o crepe nel terreno, formando flussi di lava. Le eruzioni effusive sono meno violente rispetto a quelle esplosive, ma possono comunque causare danni alle infrastrutture e modificare il paesaggio. Comprendere e studiare entrambi i tipi di eruzioni è fondamentale per prevedere e mitigare i rischi associati all'attività vulcanica e proteggere le comunità vulcaniche.

Essa produce una varietà di prodotti, come coni vulcanici e caldere, e manifestazioni vulcaniche secondarie come fumarole, soffioni, geyser, sorgenti termali e bradisismo. Questi fenomeni sono studiati per comprendere la loro formazione e comportamento. Il rischio vulcanico rappresenta una minaccia significativa per le comunità vicine ai vulcani attivi. La comprensione scientifica del vulcanismo è essenziale per prevedere e mitigare i pericoli associati alle eruzioni vulcaniche. Le autorità competenti lavorano per sviluppare piani di evacuazione, allarmi precoci e strategie di gestione del rischio. La diffusione di informazioni accurate è fondamentale per educare la popolazione sulle misure di sicurezza. La collaborazione tra scienziati, governi e comunità è fondamentale per affrontare il rischio vulcanico in modo efficace. La ricerca continua e la comunicazione giocano un ruolo chiave nella gestione del rischio vulcanico e nella protezione delle vite umane e delle infrastrutture.

-Yasmine Copoeru e Alessia Tinè
Link utilizzati: https://images.app.goo.gl/4v2kLT1tXkoMBQ6g8 https://images.app.goo.gl/5erGehzqqtzX2PGEA https://images.app.goo.gl/zJmAQAF6Ag17itb57
22 maggio 2023
Un vulcano è un'apertura naturale della crosta terrestre attraverso la quale il magma sale fino a riversarsi in superficie tramite un eruzione. È costituito sia da elementi morfologici al di sopra della superficie terrestre ( edificio vulcanico ) sia da strutture all’interno della crosta ( camera magmatica ).
I vulcani vengono distinti in:
- attivi = vulcani che hanno eruttato in epoca storica
- quiescenti = vulcani che hanno avuto eruzioni negli ultimi 10mila anni, ma che attualmente si trovano in una fase di riposo
- estinti = vulcani cui l’ultima eruzione è avvenuta oltre 10 mila anni fa
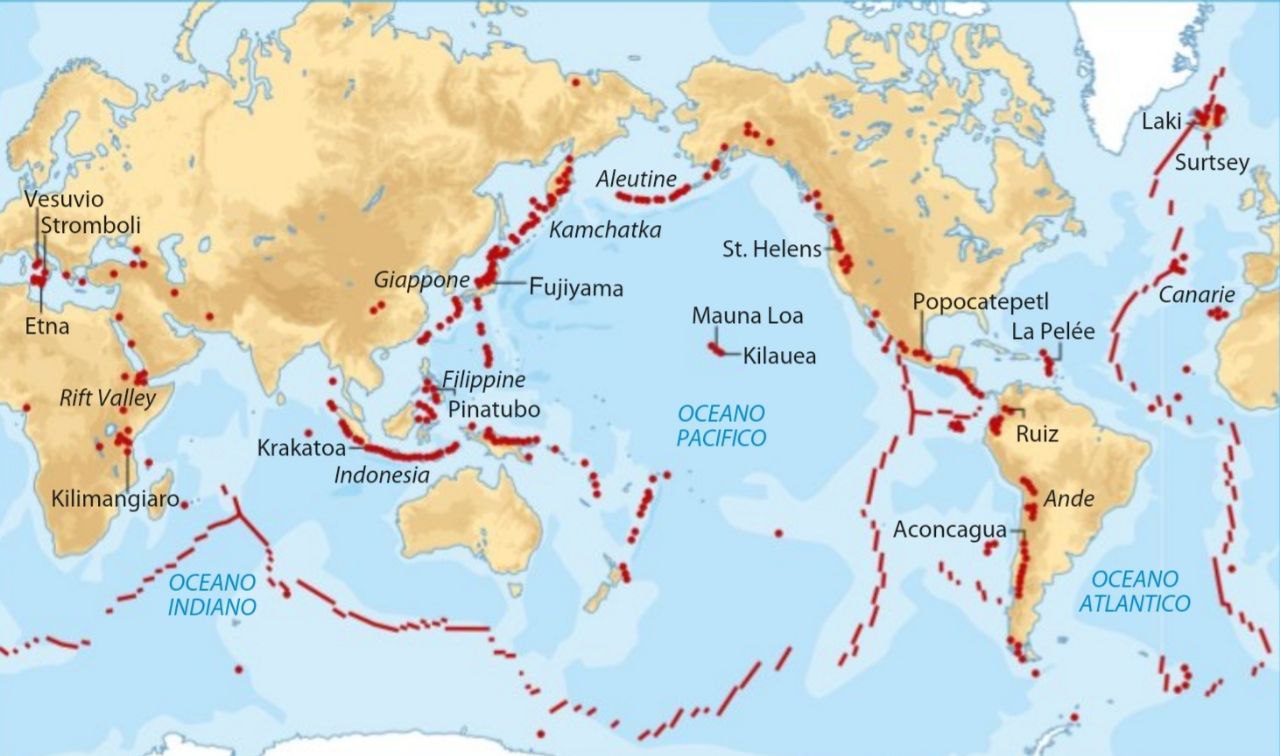
I vulcani attivi sulla terra sono circa 500-600 e non sono distribuiti in modo uniforme. La maggior parte si trova al centro degli oceani lungo le dorsali oceaniche o in corrispondenza dei margini tra le placche in cui è suddivisa la litosfera terrestre.
I magmi si formano per fusione dalle rocce tra i 30 e i 100 km di profondità. Il magma liquido si insinua nei pori delle rocce circostanti e nei piccoli spazi che trova liberi e tende a risalire. Le gocce durante lo spostamento si uniscono ad altre e formano grandi corpi di magna: i diapiri magmatici, i quali continuano a risalire finché restano meno densi delle rocce circostanti. Quando raggiungono rocce con la stessa densità si trovano in equilibrio, ma se questo equilibrio viene rotto i diapiri continuano la risalita. La rottura dell’equilibrio può essere causata da :
- apporto di nuovo magma che aumenta la temperatura \
- fusione di rocce circostanti
- cristallizzazione frazionata dei minerali più densi
Giunti in prossimità della superficie i diapiri si fermano e occupano uno spazio chiamato camera magmatica, all’interno di essa si stabilisce una condizione di equilibrio tra la pressione che esercitano le rocce sovrastanti e quella che esercitano i gas del magma.
Se questa condizione rimane stabile nel tempo il magma si raffredda e si solidifica formando rocce intrusive.
Ogni magma è caratterizzato da un contenuto di vapore acqueo e gas (idrogeno, diossido di carbonio, acido cloridrico, diossido di zolfo). Se diminuisce la pressione litostatica la solubilità dei gas diminuisce e tendono ad abbandonare il magma.
I gas e vapori che si separano dal liquido, esercitano una pressione sulle rocce sovrastanti, se la loro pressione supera un limite le rocce si frantumano e si crea il camino vulcanico. L’improvvisa diminuzione di pressione provoca l’espansione dei gas disciolti nel liquido sotto pressione.
Il magma fuoriesce in superficie sotto forma di lava dopo aver preso quasi completamente i gas che contiene.
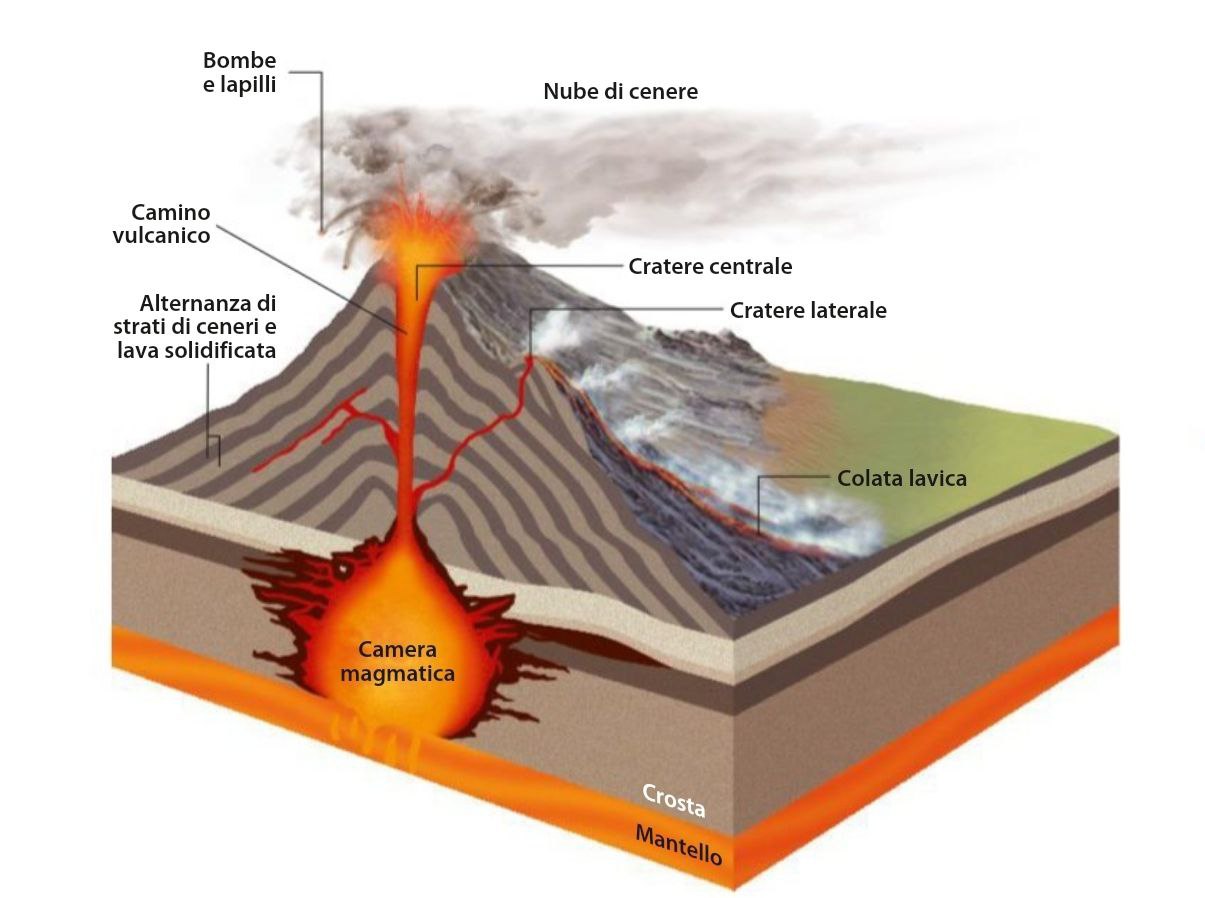
Il cratere è l’apertura attraverso la quale la lava fuoriesce. Una volta esaurita l’espansione dei gas che hanno provocato l’eruzione il condotto vulcanico viene chiuso da magma solidificato . Quanto altri gas provenienti dall’interno della terra riportano la pressione a valori critici il fenomeno si ripeterà. Le continue eruzioni vulcaniche porteranno alla formazione di un rilievo a forma di cono ovvero l’edificio vulcanico.
L’attività vulcanica può manifestarsi con modalità diverse che dipendono soprattutto dalla quantità di gas presenti nel magma e dalla sua percentuale di silice. L’abbondanza di silice,infatti, favorisce le esplosioni, mentre la scarsità di gas e il minore contenuto in silice favoriscono la formazione di colate laviche fluide ( senza esplosioni ).
Il sistema vulcano - magma può quindi essere diviso in quattro zone:
- il mantello, dove il magma si genera tramite la parziale fusione delle rocce circostanti.
- la crosta, dove il magma è circondato da rocce incassanti che variano sia come composizione, sia come storia geologica.
- la zona in cui, attraverso il camino vulcanico, il magma sale e la camera magmatica, in cui il magma stagna per un periodo più o meno lungo e si differenzia per cristallizzazione frazionata.
- l'edificio vulcanico vero e proprio, dove avviene l'eruzione in ambiente subaereo.
Le eruzioni vulcaniche possono essere divise secondo vari criteri. Una prima divisione è in quelle che scaturiscono da un condotto centrale, chiamate eruzioni centrali, da fratture o fessure, chiamate eruzioni fessurali ( o lineari ) , e quelle distribuite su grandi aree, chiamate eruzioni areali .
Un altro modo è quello di considerare le eruzioni vulcaniche in base alla loro esplosività. Vengono distinte, per esplosività crescente: le eruzioni islandiche, hawaiiane , stromboliane , vulcaniane , peleane e pliniane.
Le eruzioni islandiche sono di tipo fessurale. Sono costituite da colate di lava basaltica fluida che costruiscono vasti campi lavici piatti. Alla fine dell'eruzione si può formare una linea di piccoli coni lungo la fessura. Queste eruzioni ripetute su larga scala hanno originato i plateau basaltici, regioni caratterizzate da successioni di colate laviche estese per chilometri di spessore.
Le eruzioni hawaiiane sono caratterizzate da alte fontane di lava e da lunghe colate fluide (simili a fiumi incandescenti). A causa della fluidità del magma, i vulcani hawaiiani assumono la forma di un cono con fianchi poco inclinati, per questo sono anche chiamati vulcani a scudo. I vulcani attivi hawaiiani (il Mauna Loa, il Kilauea e il Mauna Kea) , si trovano tutti sull'Isola di Hawaii, che dà il nome all'intero arcipelago .

Le eruzioni stromboliane sono più esplosive rispetto a quelle hawaiiane. Escono dal cratere frammenti di lava incandescente che si raffreddano in scorie. Stromboli, il vulcano da cui prende il nome questo tipo di eruzione, esplode ogni 15 - 20 minuti, ed è una montagna conica , in mezzo al Tirreno, con i fianchi molto ripidi. Questo è dovuto al fatto che le eruzioni si verificano solo in corrispondenza di un condotto centrale.

Le eruzioni vulcaniche si verificano dove ci sono lave viscose che si solidificano rapidamente. Queste esplosioni sono violente e producono molta cenere vulcanica. Dopo l’iniziale fase esplosiva vengono emesse potenti colate di lava lungo i fianchi del vulcano, in questo modo si forma un cono dai fianchi ripidi detto strato - vulcano Le eruzioni peleane prendono il nome dal vulcano la Pelée. Esse sono estremamente pericolose e distruttive perché generano le nubi ardenti .

L’eruzione pliniana è un eruzione violentissima che produce una nube alta molto chilometri, caratterizzata dalla produzione di grandi quantità di cenere (in grado di seppellire intere città come pompei ).
- Laura Russo e Emanuele Miano
21 maggio 2023
Dopo aver visitato l’Etna e aver visto con i nostri occhi esemplari di rocce basaltiche…. La visita è continuata al palazzo delle scienze dell’università di Catania, in cui l’esperienza è stata divisa in due parti:
-la prima: guidati dal dottor De Giorgio, in una delle classi dell’università, abbiamo esaminato più attentamente, a occhio nudo, dei particolari tipi di rocce: sia alcune trovate qualche ora prima in natura, sia alcuni tipi di rocce non tipiche del territorio dell’etneo.
-la seconda: guidati dal dottor Russo, in un laboratorio dell’università, abbiamo avuto l’occasione di esaminare tramite dei microscopi elettronici, delle sezioni di rocce basaltiche in cui è stato facilissimo individuare e poter ammirare i minerali presenti all’interno (è stato così semplice individuare i minerali che a occhi nudo sembravano quasi impercettibili perché il microscopio elettronico ha ingrandito l’immagine della roccia di circa 300.000 volte).
Prima parte:
le rocce che abbiamo visto sono state molteplici. A partire dalle rocce già viste precedentemente sull’Etna:
basalto: è una roccia effusiva di origine vulcanica, con questo termine s’intendono tutte quelle rocce magmatiche che vengono prodotte dalla solidificazione della lava sulla superficie terrestre. Il basalto generalmente è di colore nero o comunque scuro.
Composto da plagioclasio calcico e pirosseni, oltre che da gabbro, è caratterizzato da un aspetto che va da prolifico a microcristallino o vetroso.



Come si può notare dalle foto sopra riportate, questa roccia è di colore grigio con tante “macchioline”, queste sono i minerali che possono essere di due colori: neri, chiamati “Pirosseni” appartenenti alla classe dei silicati contenenti magnesio, ferro e calcio; o verdi che prendono il nome di “Olivina” che vengono classificati come nesosilicati (particolare classe che assume una struttura cristallina composta da tetradi Z-O)
Granito: è una roccia cristallina di origine plutonica. I minerali che compongono un granito sono soprattutto quarzo e feldspato (plagioclasio e le miche ( come la biotite) sono altri minerali contenuti in abbondanza nel granito, ma secondari ai primi due citati). Questi due minerali sono i più abbondanti nella crosta terreste, perciò il granito è la roccia più presente sulla crosta terrestre.

Questa roccia si riconosce perché ha dei cristalli grandi, e ben definiti, di quarzo, feldspato, plagioclasio o mica.
Calcari organogeni: si formano per lo più in ambiente marino e derivano dall'accumulo di resti di organismi unicellulari o di gusci calcarei come le conchiglie o i gusci degli invertebrati. I gusci sono formati prevalentemente da carbonato di calcio(CaCO3), minerale noto come calcite, e sono tra le rocce organogene più importanti. Questi calcari possono formarsi principalmente ad opera di due diversi tipi di organismi:
Fitoplancton: gli organismi fotosintetici che prelevano l'anidride carbonica disciolta in acqua e fanno precipitare il carbonato di calcio, il quale viene poi trattenuto ed accumulato dagli stessi cianobatteri e batteri, che formano delle strutture carbonatiche a strati chiamate stromatoliti.
Organismi costruttori: sono ad esempio i coralli e le alghe calcaree che popolano le scogliere coralline dei mari tropicali. I polipi dei coralli, durante tutta la loro vita, prelevano il carbonato di calcio disciolto in acqua e lo fissano, creando le strutture delle costruzioni coralline.

Anfibote a granato/ortoanfioboliti:
L'anfibolite è un roccia metamorfica di colore verde o grigio scuro, formata principalmente da anfibolo orneblenda e da plagioclasio (miscela di silicati di sodio e calcio in diverse proporzioni); come componenti accessori vi sono biotite, clorite, titanite, epidoto, granato.
Assai frequente, specialmente nelle anfiboliti granatifere, è una struttura diablastica, ossia di microimplicazione tra due componenti minerali, come anfibolo orneblenda e plagioclasio, e tra granato e uno dei due precedenti.
Le anfiboliti sono collegate geneticamente, alle rocce eruttive basiche dalle quali derivano per metamorfismo e allora prendono il nome di ortoanfiboliti. Le paraanfiboliti invece derivano da rocce sedimentarie in genere marnose e in tal caso hanno una composizione mineralogica più varia. Le anfiboliti possono avere anche origine metasomatica derivando da calcari o dolomie impuri che hanno reagito con soluzionicontenenti silice, magnesio e ferro.

Seconda parte:
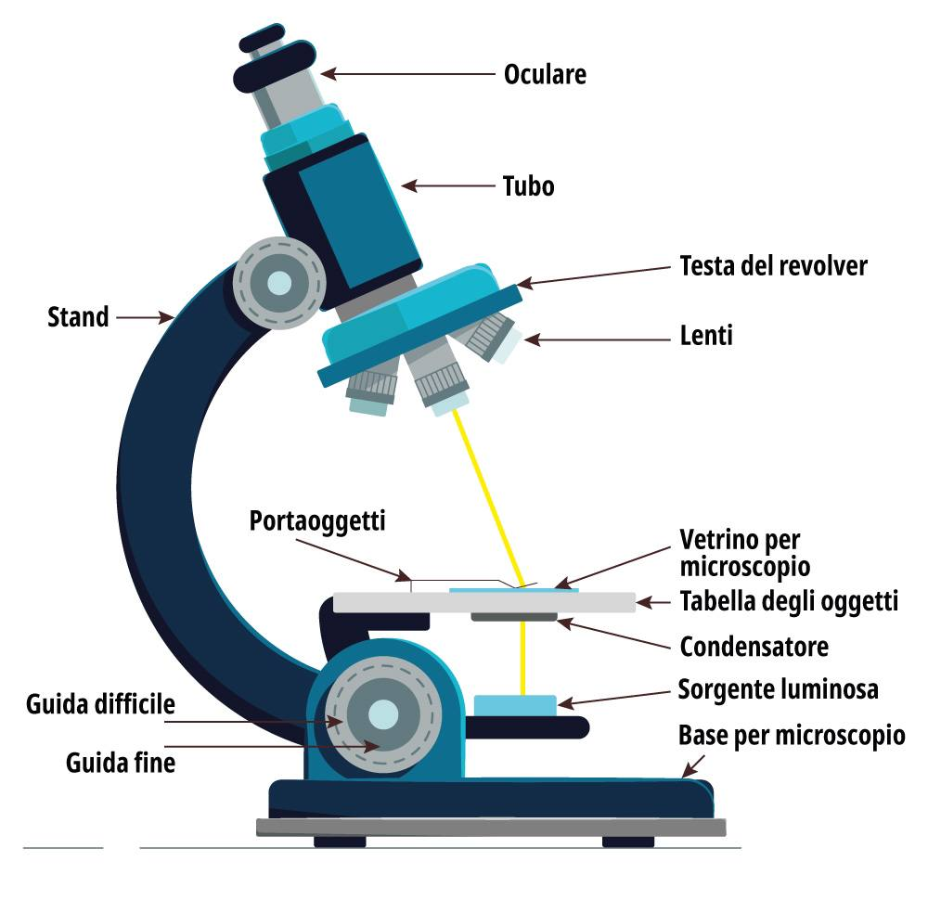
dopo una breve descrizione sul microscopio e qualche informazione sul corretto utilizzo; abbiamo subito analizzato dei vetrini:
Basalti:
I basalti sono lave solidificate che vennero a giorno a temperature anche superiori ai 1000 gradi. Quando un vulcano erutta, i suoi prodotti sono sempre in parte liquidi, in parte solidi e in parte gassosi. Nella parte solida vi sono spesso cristalli di minerali che si formano a temperature persino più alte della lava che ha formato il basalto. Questi cristalli si sono formati ad una profondità di decine di chilometri dentro la crosta terrestre. Visti al microscopio questi grandi cristalli sono nitidi e presentano colori sgargianti. La parte liquida ci appare come un aggregato di cristalli piccolissimi, che in queste immagini fanno da contorno ai cristalli più grandi. Per gli studiosi questi micro-cristalli sono importantissimi, perché ci portano notizie da profondità che non possono essere esplorate direttamente.


Plagioclasio: sono i minerali più comuni del gruppo dei feldspati, in quanto nella crosta terrestre il calcio (3.6%) è molto più abbondante del patassio (2.8%). I plagioclasi formano una soluzione solida continua tra i termini estremi albite e anortite. I plagioclasi sono stati divisi arbitrariamente in base al contenuto anortitico (in Ab wt%) in sei membri:
albite (Ab90 - Ab100), oligoclasio (Ab70 - Ab90), andesina (Ab50 - Ab70), labradorite (Ab30 - Ab50), bytownite (Ab10 - Ab30), e anortite (Ab0 - An10).
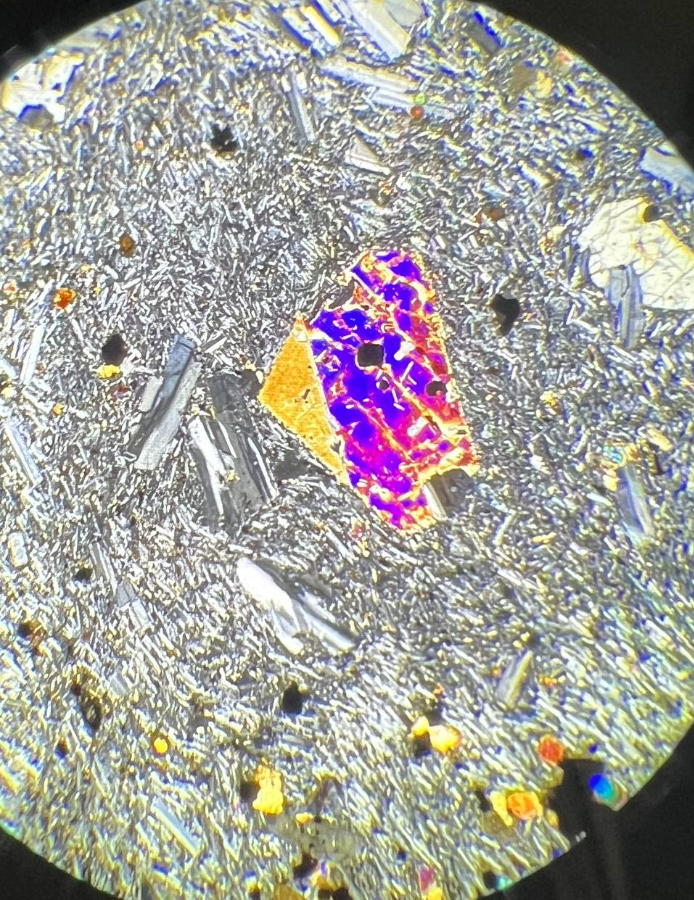
\
Tale suddivisione, pur non avendo nessun valore strutturale, è tuttavia molto utile, in quanto i plagioclasi sono minerali estremamente comuni in tutte le rocce ignee e la loro composizione varia a seconda del tipo di roccia. Ad esempio, plagioclasi sodici (oligoclasio) sono comuni in rocce acide come i graniti, plagioclasi più calcici (labradorite) sono comuni in rocce basiche come i gabbri, e plagioclasi intermedi in rocce come le sieniti e le andesiti.
\
Infine il dottor Russo ci ha illustrato una tavola, molto utile per i geologi che lavorano spesso in laboratorio, in cui sono illustrati almeno un vetrino per ogni classe di minerale, in questo modo risulta ai dottori molto più semplice riconoscere che minerale ha davanti.
- D’Alpa Nausicaa ,Martorano Camilla, Di Raimondo Renata , Larosa Marianna























































